Prueba de hidrólisis de almidón: comprensión, procedimiento y aplicaciones


La prueba de hidrólisis de almidón sirve como un método crucial para la identificación de bacterias con capacidad de hidrolizar el almidón, utilizando enzimas como la α-amilasa y la oligo-1,6-glucosidasa. El agar de hidrólisis de almidón sirve como medio en los laboratorios microbiológicos para la evaluación de la actividad enzimática de los microorganismos.
Principio de la prueba de hidrólisis del almidón
El principio de la prueba de hidrólisis del almidón radica en la detección de la capacidad de un organismo para producir la enzima amilasa, que hidroliza el almidón en subunidades más pequeñas, como maltosa y glucosa. Esta prueba ayuda a diferenciar las bacterias según su capacidad para descomponer el almidón.
Propósito del agar almidón
El agar almidón funciona como un medio diferencial destinado a probar la actividad enzimática de los microorganismos, particularmente su capacidad para producir α-amilasa y oligo-1,6-glucosidasa. Este medio evalúa la capacidad de los organismos para producir exoenzimas, que facilitan la descomposición del almidón en moléculas más pequeñas y absorbibles.
Composición y preparación de agar almidón.
El agar almidón incluye extracto de carne, almidón soluble y agar suspendido en agua destilada. El medio se esteriliza en autoclave y se vierte en placas de Petri esterilizadas para su solidificación. Además, se pueden utilizar polvo deshidratado premezclado disponible comercialmente o placas de agar prefabricadas, siguiendo las instrucciones del fabricante.
Receta de agar almidón y pautas de almacenamiento
Composición (por litro):
- Extracto de ternera: 3 g
- Almidón soluble: 10 g
- Agar: 12g
- Agua destilada: 1 litro
Preparación:
- Suspender el extracto de carne, el almidón soluble y el agar en un litro de agua destilada.
- Mezclar bien y calentar revolviendo frecuentemente hasta que hierva.
- Evite hervir excesivamente para evitar la hidrólisis del almidón.
- Autoclave a 121°C durante 15 minutos a 15 psi.
- Asegúrese de que el pH final del medio sea 7,5 ± 0,2 a 25 °C.
- Después de la esterilización, vierta el medio descongelado en placas de Petri esterilizadas (20 a 30 ml por placa) y déjelo solidificar antes de su uso.
- El medio preparado tiene un aspecto de color ámbar pálido a ligeramente opalescente.
Almacenamiento:
- Las placas de agar almidón preparadas se vuelven opacas si se enfrían.
- El medio preparado se puede dispensar en tubos con tapa de rosca y almacenar hasta por dos semanas.
- Después de dos semanas, pueden ocurrir cambios en el almidón y pueden aparecer manchas de color púrpura rojizo con la adición de yodo.
- Para usar medio almacenado en tubos, derrítalo en un baño de agua hirviendo, viértalo en platos individuales y déjelo a temperatura ambiente antes de usarlo.
- El medio de agar almidón está disponible comercialmente como polvo deshidratado premezclado o placas de agar prefabricadas de empresas de suministro biológico. Siga las instrucciones del fabricante para su preparación.
Procedimiento para la prueba de hidrólisis de almidón
1. Inoculación:
- Utilice una técnica estéril para inocular las bacterias de prueba en placas de agar almidón.
- Utilice un cultivo fresco del organismo de prueba, preferiblemente un cultivo puro de 16 a 18 horas.
- Elija una única colonia aislada y colóquela en la superficie del agar en forma de zigzag o inocúlela según corresponda.
2. Incubación:
Incubar las placas inoculadas a 35 ± 2°C durante 24 a 48 horas, o más si es necesario (hasta 3 a 5 días), permitiendo el crecimiento bacteriano y la actividad enzimática.
3. Adición de solución de yodo:
- Después del período de incubación apropiado, inunde la superficie del agar con solución de yodo de Gram usando gotas.
- Asegúrese de cubrir completamente la superficie del agar con la solución de yodo, pero evite la recolección excesiva.
- Deje que la solución de yodo reaccione con el almidón presente en el agar.
4. Visualización e Interpretación:
Observe las placas para detectar cambios de color característicos.
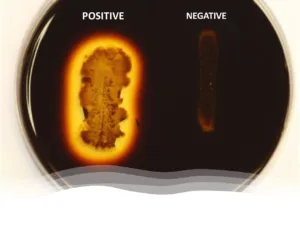
- Resultado positivo: Limpie las áreas alrededor del crecimiento bacteriano, lo que indica hidrólisis del almidón.
- Resultado negativo: Color azul oscuro o negro medio, lo que indica almidón intacto.
Registre los resultados inmediatamente para evitar interpretaciones inexactas.
Documentación:
- Documente los resultados tomando fotografías de las placas antes y después de agregar la solución de yodo.
- Etiquete claramente las placas con información relevante, incluidas las especies bacterianas, la fecha y cualquier otro detalle pertinente.
Control de calidad:
- Realice controles de calidad en cada nuevo lote de agar almidón antes de su uso.
- Asegúrese de realizar una inspección adecuada para detectar congelación, contaminación, grietas y deshidratación de las placas de agar antes de su almacenamiento y utilización.
Almacenamiento y manipulación:
- Almacenar las placas de agar almidón debidamente preparadas, evitando la exposición excesiva a la luz y manteniendo condiciones de temperatura adecuadas.
- Deseche las placas que muestren signos de deterioro, contaminación o hayan caducado.
- Siga las pautas recomendadas para los procedimientos de descontaminación y eliminación de desechos microbiológicos.
Repita la prueba (si es necesario):
- Si se obtienen resultados no concluyentes o se requiere mayor confirmación, las placas se pueden volver a incubar y analizar según sea necesario.
- Garantice la documentación adecuada y la trazabilidad de los procedimientos de prueba repetidos para mantener registros precisos.
Informes:
- Registre e informe los resultados con precisión, incluidas cualquier observación o nota adicional relevante para la interpretación de la prueba de hidrólisis del almidón.
- Comunicar los hallazgos de manera rápida y efectiva a las partes interesadas o colegas relevantes para su posterior análisis o toma de decisiones.
Resultados esperados de la prueba de hidrólisis de almidón
- Prueba positiva:
- Aparición de zonas claras: Una zona clara alrededor del crecimiento bacteriano indica hidrólisis del almidón.
- Características: El área puede aparecer inicialmente de color amarillo debido al yodo presente en el medio y progresivamente volverse más clara o clara.
- Interpretación: La presencia de zonas claras indica que el organismo de prueba tiene la capacidad enzimática de hidrolizar el almidón.
- Prueba negativa:
- Color azul oscuro o negro: El medio permanece azul oscuro o negro, lo que indica almidón intacto.
- Características: No se observan zonas claras alrededor del crecimiento bacteriano.
- Interpretación: La falta de zonas claras significa que el organismo de prueba no produce las enzimas extracelulares necesarias para hidrolizar el almidón.
Usos y limitaciones
Las pruebas de hidrólisis de almidón tienen varios propósitos, incluida la diferenciación de especies dentro de géneros bacterianos y la ayuda en la identificación de características microbianas específicas. Sin embargo, es importante reconocer sus limitaciones, como la imposibilidad de realizar subcultivos a partir de placas después de la adición de yodo debido a la muerte celular provocada por la naturaleza oxidativa del reactivo.
Conclusión:
El agar de hidrólisis de almidón representa una herramienta fundamental en los laboratorios de microbiología para la evaluación de la actividad enzimática de las bacterias y la diferenciación de especies microbianas en función de sus capacidades para degradar el almidón. Comprender los principios, procedimientos y aplicaciones de esta prueba mejora su utilidad en la identificación y caracterización de microbios y contribuye a una investigación científica y un diagnóstico clínico más amplios.
Aprende más:



