Una breve historia del átomo

átomos son pequeñas partículas de asunto que constituyen todo lo que hay en el universo. Todo lo que ves está hecho de átomos.
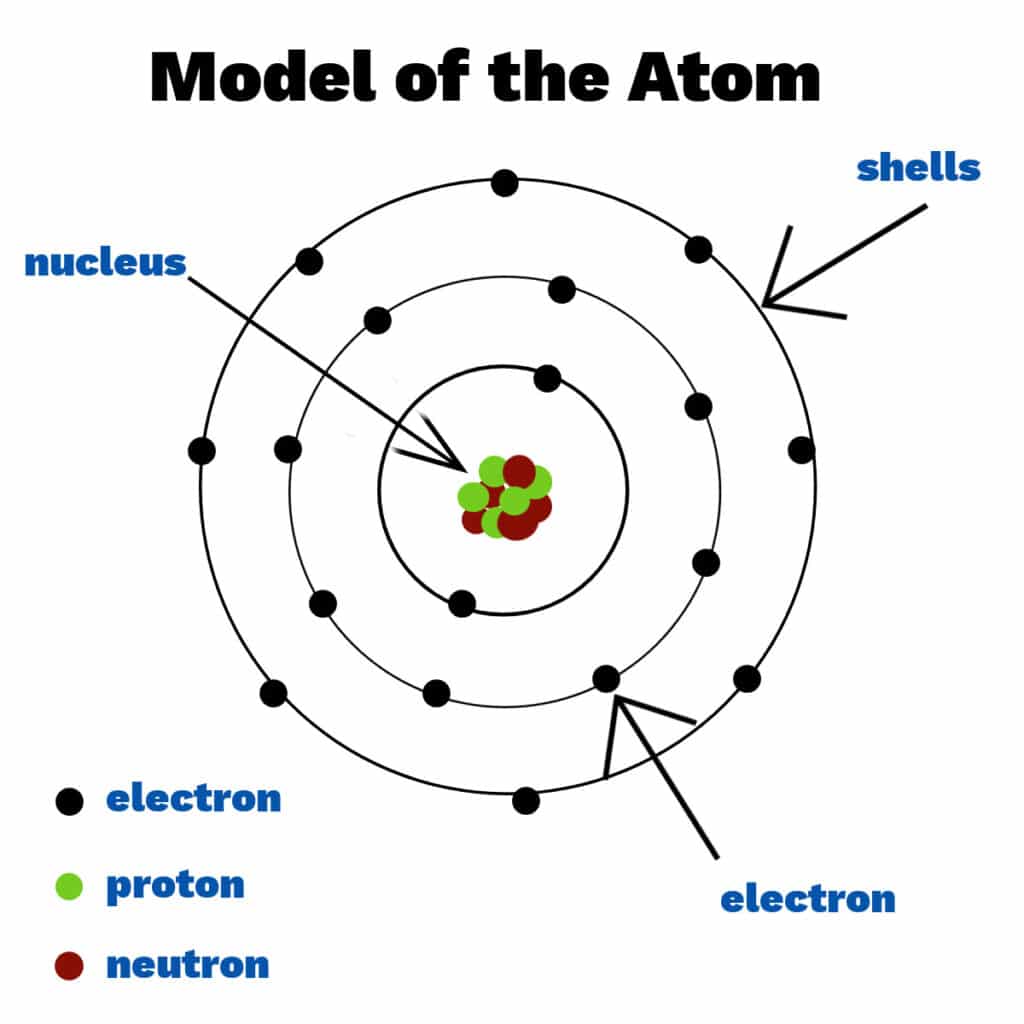
Los científicos han pasado muchos años intentando comprender la estructura del atomo, con varios modelos y teorías siendo cuestionados o mejorados a lo largo del camino. Hoy sabemos que los átomos constan de un núcleo que contiene protones y neutrones, rodeado por capas (niveles de energía) de electrones. Los electrones, protones y neutrones se conocen como partículas subatómicas. Cada capa contiene un número fijo de electrones.
Los átomos de diferentes elementos tienen diferente número de electrones, protones y neutrones.
Teoría de la estructura atómica
John Dalton
John Dalton es a menudo conocido como el padre de la teoría atómica. Propuso una teoría del átomo en 1803.
John Dalton creía que:
Toda la materia está hecha de átomos.
Los átomos eran esferas sólidas. luego disputado
Los átomos dentro de un elemento son iguales. Los átomos de diferentes elementos no lo son.
Los átomos ya no se podían romper. luego disputado
Los átomos se reorganizan durante una reacción química pero no se pierden. Este es el Ley de conservación masiva.
J.J. Thompson
En 1897, JJ Thomson propuso que los átomos no eran esferas sólidas. Su investigación demostró que los átomos deben contener partículas cargadas negativamente (electrones). Esta teoría es conocida como la Patrón de pudín de ciruela.

Ernesto Rutherford
En 1909, Ernest Rutherford y dos de sus estudiantes dirigieron el ahora infame experimento de lámina de oro. Dispararon partículas alfa cargadas positivamente contra una lámina de oro muy delgada. Si el modelo del pudín de ciruelas fuera correcto, las partículas atravesarían la lámina de oro o se desviarían muy ligeramente, ya que se pensaba que la carga se difundía a través del átomo. Se eligió el oro porque puede hacerse muy fino.
Si bien la mayoría de las partículas pasaron, algunas giraron más de lo que Rutherford esperaba y otras regresaron, lo que demuestra que el modelo del pudín de ciruelas no podía ser correcto. Rutherford desarrolló una teoría según la cual el átomo tenía un pequeño núcleo cargado positivamente en el centro con una nube de electrones negativos a su alrededor.
Las partículas alfa disparadas contra la lámina de oro se desviaron hacia atrás si estaban cerca del núcleo o atravesaron el espacio vacío del átomo.

Niels Bohr
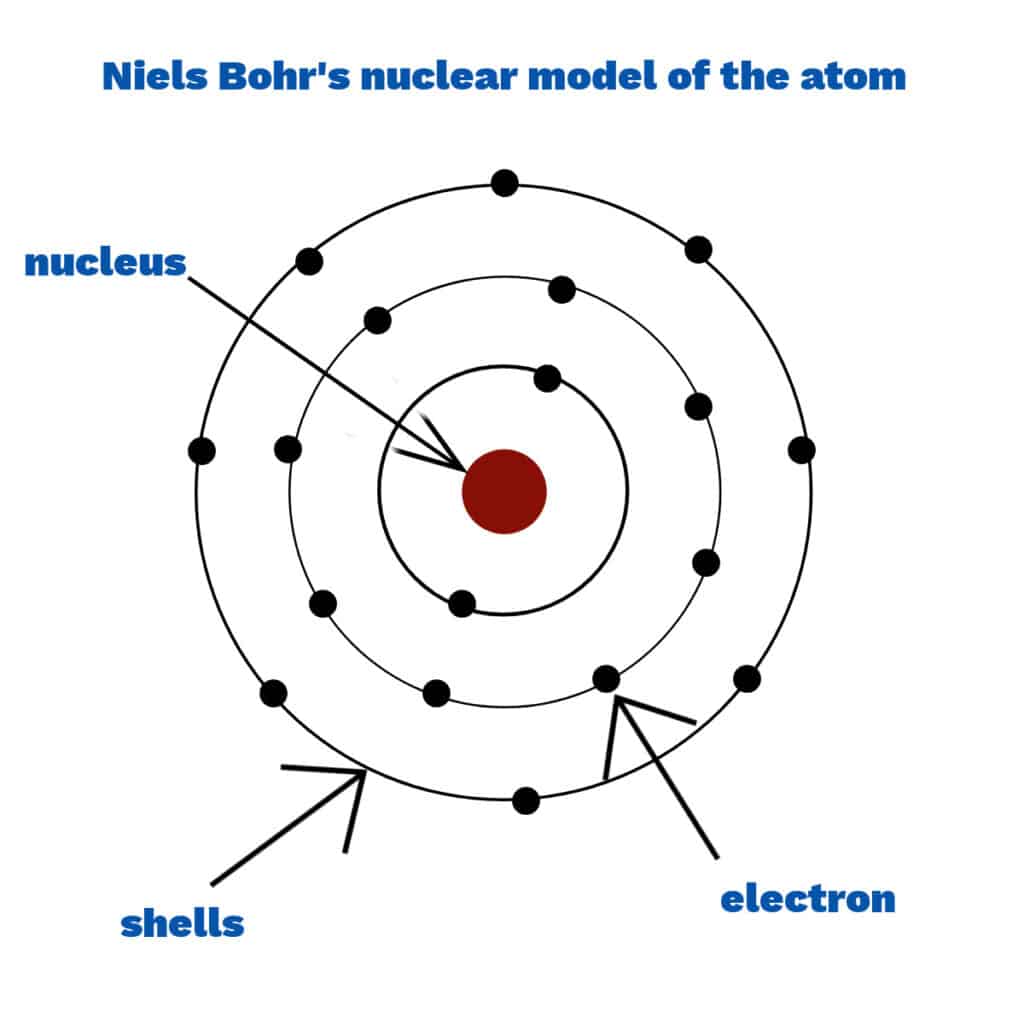
Niels Bohr desarrolló un modelo del átomo con electrones dispuestos en capas fijas alrededor del núcleo en lugar de en una nube. Los científicos pensaban que los electrones en una nube serían atraídos hacia el núcleo, provocando el colapso del átomo.

James Chadwick
James Chadwick llevó a cabo experimentos que demostraron que los átomos tienen partículas neutras (neutrones) en su núcleo. ¡El modelo de James Chadwick está muy cerca del modelo nuclear actual del átomo!

Aprende más sobre la historia del átomo.
Aprender más acerca de Ernesto Rutherfordquien recibió el Premio Nobel por su trabajo sobre la estructura atómica.
Averiguar como Ernest Schrödinger amplió el modelo propuesto por Bohr.

Última actualización el 19 de mayo de 2023 por Emma Vanstone



